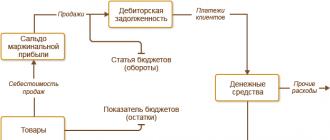
Ни для кого не секрет, что на бытовом уровне отношение к качеству воды зачастую бывает легкомысленным, основанным на вкусовой оценке «нравится - не нравится». Существуют объективные показатели качества воды, которые должны соблюдаться непосредственно при потреблении. Изначально вода стандартного качества, но по дороге к потребителю она может вобрать в себя много «лишнего».
Что такое pH?
pH - это водородный показатель, который характеризует концентрацию свободных ионов водорода в воде. Для удобства отображения был введен специальный показатель, названный рН.
pH воды - один из важнейших рабочих показателей качества воды, во многом определяющих характер химических и биологических процессов, происходящих в воде. В зависимости от величины pH может изменяться скорость протекания химических реакций, степень коррозионной агрессивности воды, токсичность загрязняющих веществ и т.д.
Обычно уровень рН находится в пределах, при которых он не влияет на потребительские качества воды. Так, в речных водах pH обычно находится в пределах 6.5-8.5, в атмосферных осадках 4.6-6.1, в болотах 5.5-6.0, в морских водах 7.9-8.3. Поэтому Всемирная Организация Здравоохранения (далее - ВОЗ) не предлагает какой-либо рекомендуемой по медицинским показателям величины для рН.
Что такое минерализация воды?
Минерализация представляет собой количественный показатель содержания растворенных в воде веществ. Этот параметр также называют содержанием растворимых твердых веществ или общим солесодержанием, так как растворенные в воде вещества находятся именно в виде солей.
По данным ВОЗ надежные данные о возможном воздействии на здоровье повышенного солесодержания отсутствуют. Поэтому по медицинским показаниям ограничения ВОЗ не вводятся. Обычно хорошим считается вкус воды при общем солесодержании до 600 мг/л, однако уже при величинах более 1000-1200 мг/л вода может вызвать нарекания у потребителей.
Вопрос о воде с низким солесодержанием также открыт. Считается, что такая вода слишком пресная и безвкусная, хотя многие тысячи людей, употребляющих обратноосмотическую воду, отличающуюся очень низким солесодержанием, наоборот находят ее более приемлемой.
Что означает «мягкая» и «жесткая» вода»?
Жесткостью называют свойство воды, обусловленное наличием в ней растворимых солей кальция и магния.
"Жесткая вода" - одна из самых распространенных проблем, причем как в загородных домах с автономным водоснабжением, так и в городских квартирах. Степень жесткости измеряется в миллиграмм-эквиваленте на литр (мг-экв/л). По американской классификации (для питьевой воды) при содержании солей жесткости менее 2 мг-экв/л вода считается "мягкой", от 2 до 4 мг-экв/л - нормальной (для пищевых целей), от 4 до 6 мг-экв/л - жесткой, а свыше 6 мг-экв/л - очень жесткой.
Для многих целей жесткость воды не играет существенной роли (например, для тушения пожаров, полива огорода, уборки улиц и тротуаров). Но в ряде случаев жесткость может создать проблемы. При принятии ванны, мытье посуды, стирке, мытье машины жесткая вода гораздо менее предпочтительна, чем мягкая. И вот почему: при использовании мягкой воды расходуется в 2 раза меньше моющих средств.
Жесткая вода, взаимодействуя с мылом, образует "мыльные шлаки", которые не смываются водой и оставляют малосимпатичные разводы на посуде и поверхности сантехники; "Мыльные шлаки" также не смываются с поверхности человеческой кожи, забивая поры и покрывая каждый волос на теле, что может стать причиной появления сыпи, раздражения, зуда.
При нагревании воды содержащиеся в ней соли жесткости кристаллизуются, выпадая в виде накипи. Накипь является причиной 90% отказов водонагревательного оборудования. Поэтому к воде, подвергаемой нагреву в котлах, бойлерах и т.п., предъявляются на поря-док более строгие требования по жесткости;
Что такое железистая вода?
Разные виды железа "ведут" себя в воде по-разному. Так, если наливаемая в сосуд вода чиста и прозрачна, но через некоторое время образуется краснобурый осадок, то это признак наличия в воде двухвалентного железа. В случае если вода уже из крана идет желтовато-бурая и образуется осадок при отстаивании - надо "винить" трехвалентное железо. Коллоидное железо окрашивает воду, но не образует осадка. Бактериальное железо проявляет себя радужной пленкой на поверхности воды и желеобразной массой, накапливаемой внутри труб.
Необходимо также отметить, что "беда никогда не ходит одна" и на практике почти всегда встречается сочетание нескольких или даже всех видов железа. Учитывая, что нет единых утвержденных методик определения органического, коллоидного и бактериального железа, то в деле подбора эффективного метода (или комплекса метдов) очистки воды от железа очень много зависит от практического опыта фирмы, занимающейся водоочисткой.
Методы удаления железа из воды
Удаление из воды железа - без преувеличения одна из самых сложных задач в водоочистке. Каждый из существующих методов применим только в определенных пределах, и имеет как достоинства, так и существенные недостатки. Выбор конкретного метода удаления железа (или их комбинации) в большей степени зависит от опыта водоочистной компании. Не без гордости можем сообщить, что нам в своей практике неоднократно приходилось сталкиваться с содержанием железа в 20-35 мг/л и успешно удалять его.
Итак, к существующим методам удаления железа можно отнести:
1. Окисление (кислородом воздуха или хлором, перекисью водорода, озоном) с последующим осаждением и фильтрацией. Это наиболее старый способ и используется только на крупных муниципальных системах. Наиболее передовым и сильным окислителем на сегодняшний день является озон. Однако установки для его производства довольно сложны, дороги и требуют значительных затрат электроэнергии, что ограничивает его применение.
У всех перечисленных способов окисления есть ряд недостатков:
Во-первых, если не применять коагулянты, то процесс осаждения окисленного железа занимает долгое время, в противном же случае фильтрация некоагулированных частиц сильно затрудняется из-за их малого размера.
Во-вторых, эти методы окисления слабо помогают в борьбе с органическим железом.
В-третьих, наличие в воде железа часто сопровождается наличием марганца. Марганец окисляется гораздо труднее, чем железо и, кроме того, при значительно более высоких уровнях рН.
2. Каталитическое окисление с последующей фильтрацией. Наиболее распространенный на сегодняшний день метод удаления железа, применяемый в компактных высокопроизводительных системах.
Суть метода заключается в том, что реакция окисления железа происходит на поверхности гранул специальной фильтрующей среды, обладающей свойствами катализатора (ускорителя химической реакции окисления).
Все системы на основе данного типа окисления кроме специфических черт имеют и ряд недостатков:
Во-первых. Они неэффективны в отношении органического железа.
Во-вторых, системы этого типа все равно не могут справиться со случаями, когда содержание железа в воде превышает 15-20 мг/л, что совсем не редкость. Присутствие в воде марганца только усугубляет ситуацию.
3. Ионный обмен. Ионный обмен как метод обработки воды известен довольно давно и применялся (да и теперь применяется) в основном для умягчения воды. Достоинством ионного обмена является также и то, что он "не боится" верного спутника железа - марганца, сильно осложняющего работу систем, основанных на использовании методов окисления. Главное же преимущество ионного обмена в том, что из воды могут быть удалены железо и марганец, находящиеся в растворенном состоянии.
Однако на практике, возможность применения катионообменных смол по железу, бывает сильно затруднена.
Объясняется это следующими причинами:
Во-первых, ионообменные смолы очень критичны к наличию в воде трехвалентного железа, которое "забивает" смолу и очень плохо из нее вымывается.
Во-вторых, при высокой концентрации в воде железа, с одной стороны возрастает вероятность образования нерастворимого трехвалентного железа, и, с другой стороны, гораздо быстрее истощается ионообменная ёмкость смолы.
В-третьих, наличие в воде органических веществ (в том числе и органического железа) может привести к быстрому "зарастанию" смолы органической пленкой, которая служит питательной средой для бактерий.
Тем не менее, именно применение ионообменных смол представляется наиболее перспективным направлением в деле борьбы с железом и марганцем в воде.
4. Мембранные методы. Мембранные технологии достаточно широко используются в водоподготовке, однако удаление железа отнюдь не главное их предназначение. Этим и объясняется тот факт, что применение мембран пока не входит в число стандартных методов борьбы с присутствием в воде железа. Основное назначение мембранных систем - удаление бактерий, простейших и вирусов, подготовка высококачественной питьевой воды. То есть они предназначены для глубокой доочистки воды.
Практическое же применение мембран ограничено следующими факторами:
Во-первых, мембраны даже в большей степени, чем гранулированные фильтрующие среды и ионообменные смолы, критичны к "зарастанию" органикой и забиванию поверхности нерастворимыми частицами (в данном случае ржавчиной). То есть мембранные системы применимы либо там, где нет железа, либо проблема с этими загрязнениями должна быть предварительно решена другими методами.
Во-вторых, стоимость. Мембранные системы весьма и весьма недешевы. Их применение рентабельно только там, где требуется очень высокое качество воды (например, в пищевой промышленности).
Что такое окисляемость?
Окисляемость - это величина, характеризующая содержание в воде органических и минеральных веществ, окисляемых одним из сильных химических окислителей.
Выражается этот параметр в миллиграммах кислорода, участвовшего в окислении этих веществ, содержащихся в 1 дм3 воды.
Наиболее высокая степень окисления достигается бихроматным и иодатным методами. Величина окисляемости природных вод может варьироваться в широких пределах от долей миллиграммов до десятков миллиграммов О2 на литр воды.

Поверхностные воды имеют более высокую окисляемость по сравнению с подземными. Так, горные реки и озера характеризуются окисляемостью 2-3 мг О2/дм3, реки равнинные - 5-12 мг О2 /дм3. Подземные же воды имеют в среднем окисляемость на уровне от сотых до десятых долей миллиграмма О2 /дм3.
Как нормируются чувственные показатели качества воды?
К числу органолептических (или чувственных) показателей относятся те параметры качества воды, которые определяют ее потребительские свойства, т.е. те свойства, которые непосредственно влияют на органы чувств человека (обоняние, осязание, зрение). Наиболее значимые из этих параметров - вкус и запах - не поддаются формальному измерению, поэтому их определение производится экспертным путем. Работа экспертов, дающих оценку органолептическим свойствам воды, очень сложна и ответственна и во многом сродни работе дегустаторов самых изысканных напитков, так как они должны улавливать малейшие оттенки вкуса и запаха.
Запах и привкус
Химически чистая вода совершенно лишена вкуса и запаха. Однако в природе такая вода не встречается - она всегда содержит в своем составе растворенные вещества. По мере роста концентрации неорганических и органических веществ, вода начинает принимать тот или иной привкус и/или запах.
Основными причинами возникновения привкуса и запаха в воде являются:
- Гниющие растения. Водоросли и водные растения в процессе гниения могут взывать рыбный, травяной, гнилостный запах воды.
- Грибки и плесень. Эти микроорганизмы вызывают возникновение плесневого, зем-листого или затхлого запаха и привкуса.
- Железистые и сернистые бактерии.
- Железо, марганец, медь, цинк. Продукты коррозии этих металлов придают воде характерный резкий привкус.
- Хлорирование воды. Вопреки широко распространенному мнению, сам хлор при правильном использовании не вызывает возникновения сколько-нибудь заметного запаха или привкуса. Появление же такого запаха/привкуса свидетельствует о передозировке при хлорировании. В то же время, хлор способен вступать в химические реакции с различными растворенными в воде веществами, образуя при этом соединения, которые собственно и придают воде хорошо известный многим запах и привкус "хлорки".
Цветность
Цветность определяется путем сравнения окраски испытуемой воды с эталонами и выражается в градусах платиново-кобальтовой шкалы. Различают "истинный цвет", обусловленный только растворенными веществами, и "кажущийся" цвет, вызванный присутствием в воде коллоидных и взвешенных частиц.
Цветность природных вод обусловлена в основном присутствием окрашенных органических веществ и соединений железа и некоторых других металлов.
Наибольшую цветность имеют поверхностные воды рек и озер, расположенных в зонах торфяных болот и заболоченных лесов, наименьшую - в лесостепях и степных зонах.
Мутность
Мутность воды вызвана присутствием веществ органического и неорганического происхождения.
В России мутность воды определяют фотометрическим путем сравнения проб исследуемой воды со стандартными суспензиями. Результат измерений выражают в мг/дм3 при использовании основной стандартной суспензии каолина или в ЕМ/дм3 (едини-цы мутности на дм3) при использовании основной стандартной суспензии формазина.
Общее микробное число
В связи с тем, что определение патогенных бактерий при биологическом анализе воды представляет собой непростую и трудоемкую задачу, в качестве критерия бактериологической загрязненности используют подсчет общего числа образующих колонии бактерий (Colony Forming Units - CFU) в 1 мл воды. Полученное значение называют общим микробным числом.
В основном для выделения бактерий и подсчета общего микробного числа используют метод фильтрации через мембрану.
При этом методе определенное количество воды пропускается через специальную мембрану. В результате, на поверхности мембраны остаются все находящиеся в воде бактерии. После чего мембрану с бактериями помещают на определенное время в специальную питательную среду при температуре 30-37 оС.
Во время этого периода, называемого инкубационным, бактерии получают возможность размножиться и образовать хорошо различимые колонии, которые уже легко поддаются подсчету.
Колиформные бактерии
Термин "Колиформные организмы" (или "колиформные бактерии") относится к классу бактерий, имеющих форму палочек, в основном живущих и размножающихся в нижнем отделе пищеварительного тракта человека и большинства теплокровных животных (например, домашнего скота и водоплавающих птиц).
В воду попадают, как правило, с фекальными стоками и способны выживать в ней в течение нескольких недель, хотя и лишены способности к размножению.
Известное выражение диетологов: «Мы есть то, что мы едим» можно перефразировать в отношении воды. Наше здоровье напрямую зависит от того, что мы пьем. К сожалению, качество питьевой воды вызывает серьезную обеспокоенность во всем мире. Состояние водопроводных систем заставляет все чаще прибегать к установке мощных фильтров или к употреблению покупной бутилированной воды. Какую воду мы называем минеральной? Как влияет минерализация вод на здоровье человека?
Какая вода может называться минеральной?
Обычную питьевую воду, которую мы набираем из-под крана, или покупаем в бутылях, тоже можно считать, в некоторой степени, минеральной. В ней тоже в разных пропорциях присутствуют соли и различные химические элементы. И все-таки под определенным названием принято подразумевать воду, насыщенную полезными органическими веществами в разной степени концентрации. Основным показателем, определяющим химический состав основного источника жизни, его пригодность для питья, является общая минерализация воды или, по-другому, сухой остаток. Это показатель количества органических веществ в одном литре жидкости (мг/л).
Источники минерализации
Минерализация вод может происходить как естественным природным путем, так и промышленным, искусственно. В природе подземные реки принимают в свой состав ценные соли, микроэлементы и прочие частицы из пород, по которым они проходят.
Чистые питьевые источники, увы, стали редкостью. Человечество все чаще вынуждено применять специальные установки для их очистки от загрязнений вредными веществами. Современные методы фильтрации могут извлечь пригодную для употребления воду практически из любой жидкости. В результате применения таких технологий она порой становится почти дистиллированной и тоже вредной для постоянного использования в пищу. Искусственно очищенная вода проходит повторную минерализацию и наполняется необходимым составом уже ненатуральным способом.

Степень минерализации воды
Вода с показателем сухого остатка ниже 1000 мг/л считается пресной, такой показатель большинства рек и озер. Именно этот порог считается наивысшим для питьевой воды, на этом пределе человек не ощущает дискомфорта и неприятного соленого или горького вкуса. Минерализация воды выше 1000 мг/л, кроме того, что меняет ее вкус, понижает способность утолять жажду, и порой оказывает вредное воздействие на организм.
Ниже 100 мг/л - низкая степень минерализации. Такая вода имеет неприятный вкус, вызывает нарушения в обмене веществ при длительном ее употреблении.
Учеными бальнеологами выведен оптимальный показатель насыщенности органическими веществами - от 300 до 500 мг/л. Сухой остаток от 500 до 100 мг/л считается повышенным, но допустимым.

Потребительские свойства воды
По своим потребительским свойствам воду следует разделить на пригодную для ежедневного употребления, и ту, которая используется в лечебно-профилактических целях.
- Очищенная искусственным путем от всех веществ вода пригодна для питья и приготовления пищи. Вреда большого она не принесет, кроме того, что не принесет абсолютно никакой пользы. Те, кто, боясь инфекций, употребляет только такую жидкость, рискуют получить дефицит полезных солей и минералов. Пополнять их придется искусственно.
- Столовая вода - самая благоприятная для ежедневного употребления, очищенная от грязи и вредных примесей и умеренно напитанная всем необходимым.
- Лечебно-столовые воды уже отличаются приставкой «лечебно». Принимают их как лекарство или для профилактики. То есть пить их можно всем, но умеренно и не постоянно, а вот для приготовления пищи использовать нельзя.
- Сугубо лечебные минводы обычно принимают только по назначению врача, в большинстве случаев как процедуру на бальнеологическом курорте. Высокая минерализация воды делает ее употребление неприемлемым в широком кругу.

Классификация воды по составу
В обществе минеральной принято называть лечебные и лечебно-столовые растворенных в них органических веществ, минералов и газов значительно отличается и зависит от места нахождения источника. Основная характеристика воды - ее ионный состав, в общий перечень которого входит около 50 различных ионов. Основная минерализация вод представлена шестью основными элементами: катионами калия, кальция, натрия и магния; анионами хлорида, сульфата и гидрокарбоната. По преобладанию тех или иных элементов и делят минводы на три большие основные группы: гидрокарбонатные, сульфатные и хлоридные.
В большинстве случаев в чистом виде отдельная группа воды представлена в природе редко. Чаще всего встречаются источники смешанного типа: хлоридно-сульфатные, сульфатно-гидрокарбонатные и т.д. В свою очередь, группы делятся на классы по преобладанию тех или иных ионов. Есть воды кальциевые, магниевые или смешанные.

Просто пей и будь здоров
Минерализация вод широко используется в медицинских целях, как для внутреннего применения, так и для наружного, в виде ванн и других водных процедур.
- Гидрокарбонатные воды применяют для лечения и профилактики заболеваний органов пищеварения, связанных с повышенной кислотностью. Они помогают избавиться от изжоги, очищают организм от песка и камней.
- Сульфаты также стабилизируют работу кишечника. Основная область их воздействия - печень, желчные пути. Рекомендуют лечение такими водами при сахарном диабете, ожирении, гепатите, непроходимости желчных путей.
- Наличие хлоридов устраняет расстройства желудочно-кишечного тракта, стабилизирует работу желудка и поджелудочной железы.
Высокой минерализации может нанести и заметный ущерб здоровью, если применять ее неправильно. Человеку с проблемами пищеварения и обмена веществ следует принимать эти природные лекарства по назначению и под контролем медперсонала.
Минерализация, общее солесодержание (TDS)
- Большинство рек имеет минерализацию от нескольких десятков миллиграммов в литре до нескольких сотен. Их удельная электропроводность варьируется в пределах от 30 мкСим/см до 1500 мкСим/см.
- Минерализация подземных вод и соленых озер изменяется в интервале от 40-50 мг/дм 3 до 650 г/кг (плотность в этом случае уже значительно отличается от единицы).
- Удельная электропроводность атмосферных осадков (с минерализацией от 3 до 60 мг/дм 3) составляет величины 20-120 мкСим/см.
Многие производства, сельское хозяйство, предприятия питьевого водоснабжения предъявляют определенные требования к качеству вод, в частности, к минерализации, так как воды, содержащие большое количество солей, отрицательно влияют на растительные и животные организмы, технологию производства и качество продукции, вызывают образование накипи на стенках котлов, коррозию, засоление почв.
Классификация природных вод по минерализации.
В соответствии с гигиеническими требованиями к качеству питьевой воды суммарная минерализация не должна превышать величины 1000 мг/дм 3 . По согласованию с органами Роспотребнадзора для водопровода, подающего воду без соответствующей обработки (например, из артезианских скважин), допускается увеличение минерализации до 1500 мг/дм 3).
Удельная электропроводность воды
Удельная электропроводность - это численное выражение способности водного раствора проводить электрический ток. Электрическая проводимость природной воды зависит в основном от концентрации растворенных минеральных солей и температуры. Природные воды представляют в основном растворы смесей сильных электролитов. Минеральную часть воды составляют ионы Na + , K + , Ca 2+ , Cl - , SO 4 2- , HCO 3 - . Этими ионами и обуславливается электропроводность природных вод. Присутствие других ионов, например, Fe 3+ , Fe 2+ , Mn 2+ , Al 3+ , NO 3 - , HPO 4 2- , H 2 PO 4 - не сильно влияет на электропроводность, если эти ионы не содержатся в воде в значительных количествах (например, ниже выпусков производственных или хозяйственно-бытовых сточных вод). По значениям электропроводности природной воды можно приближенно судить о минерализации воды с помощью предварительно установленных зависимостей. Затруднения, возникающие при оценке суммарного содержания минеральных веществ (минерализации) по удельной электропроводности связаны с:
- неодинаковой удельной электропроводимостью растворов различных солей;
- повышением электропроводимости с увеличением температуры.
Нормируемые величины минерализации приблизительно соответствуют удельной электропроводности 2 мСим/см (1000 мг/дм 3) и 3 мСим/см (1500 мг/дм 3) в случае как хлоридной (в пересчете на NaCl), так и карбонатной (в пересчете на CaCO 3) минерализации. Величина удельной электропроводности служит приблизительным показателем их суммарной концентрации электролитов, главным образом, неорганических, и используется в программах наблюдений за состоянием водной среды для оценки минерализации вод. Удельная электропроводность - удобный суммарный индикаторный показатель антропогенного воздействия.
Температура
Температура воды является результатом нескольких одновременно протекающих процессов, таких как солнечная радиация, испарение, теплообмен с атмосферой, перенос тепла течениями, турбулентным перемешиванием вод и др. Годовой и суточный ход температуры воды на поверхности и глубинах определяется количеством тепла, поступающего на поверхность, а также интенсивностью и глубиной перемешивания. Суточные колебания температуры могут составлять несколько градусов и обычно проникают на небольшую глубину. На мелководье амплитуда колебаний температуры воды близка к перепаду температуры воздуха. В требованиях к качеству воды водоемов, используемых для купания, спорта и отдыха, указано, что летняя температура воды в результате спуска сточных вод не должна повышаться более, чем на 3 °С по сравнению со среднемесячной температурой самого жаркого месяца года за последние 10 лет. В водоемах рыбохозяйственного назначения допускается повышение температуры воды в результате спуска сточных вод не больше, чем на 5 °С по сравнению с естественной температурой. Температура воды - важнейший фактор, влияющий на протекающие в водоеме физические, химические, биохимические и биологические процессы, от которого в значительной мере зависят кислородный режим и интенсивность процессов самоочищения. Значения температуры используют для вычисления степени насыщения воды кислородом, различных форм щелочности, состояния карбонатно-кальциевой системы, при многих гидрохимических, гидробиологических, особенно лимнологических исследованиях, при изучении тепловых загрязнений.
Растворенных веществ (неорганические соли, органические вещества). Так же этот показатель называют содержанием твердых веществ или общим солесодержанием . Растворенные газы при вычислении общей минерализации не учитываются.
За рубежом минерализацию так же называют «общим количеством растворенных частиц» - Total Dissolved Solids (TDS).
Наибольший вклад в общую минерализацию воды вносят распространенные неорганические соли (бикарбонаты, хлориды и сульфаты кальция, магния, калия и натрия), а также небольшое количество органических веществ.
Единицы измерения
Обычно минерализацию подсчитывают в миллиграммах на литр (мг/л), но, учитывая, что единица измерения "литр" не является системной, правильнее минерализацию выражать в мг/куб.дм, при больших концентрациях - в граммах на литр (г/л, г/куб.дм). Также уровень минерализации может выражаться в частицах на миллион частиц воды - parts per million (ppm). Соотношение между единицами измерения в мг/л и ppm почти равное и для простоты можно принять, что 1 мг/л = 1 ppm .
Классификация
В зависимости от общей минерализации воды делятся на следующие виды :
- слабоминерализованные (1-2 г/л),
- малой минерализации (2-5 г/л),
- средней минерализации (5-15 г/л),
- высокой минерализации (15-30 г/л) ,
- рассольные минеральные воды (35-150 г/л)
- крепкорассольные воды (150 г/л и выше).
Источники минерализации вод
На минерализацию вод влияют как природные факторы, так и воздействие человека. Природная минерализация зависит от геологии района происхождения вод. Различный уровень растворимости минералов природной среды оказывает серьезное влияние на итоговую минерализацию воды.
Воздействие человека сводится к сточным водам промышленности, городским ливневым стокам (т.к. соли и прочие химреагены используется зимой для борьбы с оледенением дорожного покрытия), стокам с сельхозугодий (которые обрабатываются химическими удобрениями) и т.п.
Питьевая вода
Качество питьевой воды регулируется в России рядом стандартов, а именно:
Источники
См. также
Wikimedia Foundation . 2010 .
Синонимы :Смотреть что такое "Минерализация" в других словарях:
- (франц., от mineral минерал). Превращение в твердое тело, в ископаемое; образование камней и руд. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. МИНЕРАЛИЗАЦИЯ пропитывание дерева или тканей минеральными солями.… … Словарь иностранных слов русского языка
минерализация - и, ж. minéralisation f. 1. геол. Процесс образования руд и камней. Уш. 1938. Сии минеральныя изпарения всего более участвуют в кристаллизации, крашении камней и минерализации. Карамзин ДВ 12 164. // Сл. 18. || Минеральное тело, минерал. Сл. 18.… … Исторический словарь галлицизмов русского языка
МИНЕРАЛИЗАЦИЯ, процесс образования ИСКОПАЕМЫХ, при котором органические компоненты организма замещаются неорганическим веществом. Циркулирующая вода растворяет определенные компоненты костей и панцирей, которые замещаются кремнеземом, железом или … Научно-технический энциклопедический словарь
Процесс привноса, а также отложения рудных и нерудных м лов восходящими или нисходящими рудоносными растворами или газовыми эманациями, а иногда и магм. расплавами. Часто под этим словом понимается результат процесса отложения м лов, т. е.… … Геологическая энциклопедия
МИНЕРАЛИЗАЦИЯ, минерализации, мн. нет, жен. Процесс образования руд и камней (геол.). || Насыщение органических тел минералами; образование окаменелостей (палеонт.). Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
Превращение (расщепление, окисление) органических веществ в неорганические. Обычно происходит при участии микроорганизмов, обеспечивающих круговорот биогенных элементов в природе. (Источник: «Микробиология: словарь терминов», Фирсов Н.Н., М:… … Словарь микробиологии
Сущ., кол во синонимов: 2 окаменение (18) петрификация (5) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Минерализация - концентрация солей в водах; выражается в мг/л, г/л. Один из важнейших показателей загрязнения... Источник: МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРОВЕДЕНИЮ ИНЖЕНЕРНО ЭКОЛОГИЧЕСКИХ ИЗЫСКАНИЙ ДЛЯ ЦЕЛЕЙ РЕКУЛЬТИВАЦИИ СУЩЕСТВУЮЩИХ СВАЛОК И ПРОЕКТИРОВАНИЯ… … Официальная терминология
минерализация - Процесс разложения погребенного тела на отдельные химические элементы и простые химические соединения. Примечание Период минерализации определяется климатическими, почвенными, ландшафтными и т.п. условиями места расположения кладбища. [ГОСТ Р… … Справочник технического переводчика
минерализация - 2.10.7 минерализация: Процесс разложения погребенного тела на отдельные химические элементы и простые химические соединения. Примечание Период минерализации определяется климатическими, почвенными, ландшафтными и т.п. условиями места… … Словарь-справочник терминов нормативно-технической документации
Книги
- Сульфидная, стронциевая и редкоземельная минерализация фоскоритов и карбонатитов Турьинского массива и месторождения Люлекоп , П. И. Карчевский , Приводятся результаты детального исследования парагенети-ческих ассоциаций, физических свойств и химического состава сульфидов в фоскоритах и карбонатитах одного из крупнейшего на Кольском… Категория: Геология. Полезные ископаемые Издатель:
7. ХИМИЧЕСКИЙ СОСТАВ ПОДЗЕМНЫХ ВОД И ОЦЕНКА ИХ
КАЧЕСТВА
7.1. Формы выражения результатов анализа химического состава
подземных вод
Природная вода − сильнейший растворитель минералов и горных пород, обогащена различными солями. В связи с большим разбавлением природных растворов, соли практически полностью диссоциированы на ионы.
Главными ионами являются катионы Са2+, Mg2+, Na++К+, и анионы НСО3-, SO42-, Cl-. Определение содержания ионов выполняется аналитическими методами. Результаты принято представлять в ионной, эквивалентной и процентной формах (таблица 6).
Ионная форма - выражение содержания в природных водах ионов в единицах массы на определенный объем воды. Обычно это миллиграммы или граммы на литр воды. Ионная форма дает массовое содержание данного вещества в воде, что имеет большое практическое значение.
Эквивалентная форма. Ионы взаимодействуют друг с другом в эквивалентных количествах. Поэтому для установления взаимосвязи между ионами анализы выражают в эквивалентной форме. Она позволяет:
Судить о правильности произведенного анализа;
Составить гипотетические соли;
Классифицировать воды по ряду показателей.
Для пересчета необходимо содержание иона в мг/л разделить на его эквивалентный вес или умножить на пересчетный коэффициент, который является величиной обратной эквивалентному весу (таблица 7).
В природных водах ион Na+ значительно преобладает по сравнению с К+, поэтому сумма ионов (Na++К+) определяют по условному коэффициенту 0,04 (или по Na+).
|
Эквивалентный вес |
Пересчетный коэффициент |
Эквивалентный вес |
Пересчетный коэффициент |
||
Таблица 7 − Эквивалентные веса и пересчетные коэффициенты
Контроль анализа. Суммы анионов и катионов в мг-экв/л должны быть равны или незначительно различаться. Допустимая погрешность находится по формуле:
где ΣА – сумма анионов в мг-экв/л;
ΣК – сумма катионов в мг-экв/л.З0
В нашем примере расчет А доп производим для 10 и 11 скважин:
Погрешность допустимая;
Погрешность допустимая.
Процент-эквивалетная форма (%-экв) удобна для последующих сопоставлений природных вод различной минерализации и более четкого представления о соотношениях между ними. Процент-эквивалентная форма используется при графической обработке данных анализа, классификации вод и оценке их качества.
Для вычисления необходимо сумму эквивалентов катионов (ΣК ) и сумму эквивалентов анионов (ΣА ), каждую в отдельности, принять за 100 %, а затем рассчитать процентное содержание каждого иона. Точность расчета – до одного знака после запятой.
Проверку расчета проводят суммируя %-эквивалентные содержания анионов и катионов отдельно, суммы должны быть равны 100 %-экв.
7.2. Определение минерализации воды
Минерализация – количество растворенных в воде минеральных веществ выраженное в мг/л или г/л. Она имеет следующие понятия:
- сумма ионов (ΣИ , г/л) – арифметическая сумма содержания всех определенных анализом ионов в мг/л или г/л;
- сухой остаток определяется экспериментально, путем выпаривания определенного объема воды и высушивания осадка при температуре 110 о С.
Контроль анализа выполняется по сопоставлению величин сухого остатка и суммы ионов: они должны отличаться на 0,5 НСО 3 - . Это объясняется тем, что при нагревании ионы НСО 3 - переходят в СО 3 2- по схеме:
2НСО 3 - →СО 3 2- + Н 2 О + СО 2 ,
т. е. вместо 2 ионов НСО 3 - в сухом остатке остается только один ион СО 3 2- .
Согласно ГОСТ 17403-72 природные воды по минерализации разделены на группы (таблица 8). Предел пресных вод – 1 г/кг – установлен в связи с тем, что при минерализации более этого значения вкус воды неприятен – соленый или горько-соленый.
Таблица 8 – Характеристика вод по минерализации
7.3. Определение жесткости воды
Жесткость воды, согласно стандарту выражается суммой мг-экв/л ионов Са 2+ и Mg 2+ . Различают общую, устранимую (карбонатную) и неустранимую (постоянную) жесткость.
Общая жесткость равна сумме концентраций находящихся в воде катионов Са 2+ и Mg 2+ :
r Са 2+ + rMg 2+ = общая жесткость(мг-экв/л),где r - содержание иона в мг-экв/л.
Устранимая жесткость определяется по содержанию в воде гидрокарбонат-иона. При кипячении часть ионов Са 2+ и Mg 2+ соединяется с равным количеством иона НСО 3 - и образует накипь.
Неустранимая жесткость связана с наличием в воде солей сильных кислот Са 2+ и Mg 2+ (хлоридов, сульфатов, нитратов и т.д.) Определяется как разность общей и устранимой жесткости:
r Са 2+ + rMg 2+ − r НСО 3 - - жесткость неустранимая.
Определяют общую жесткость воды в соответствии с классификацией (таблица 9).
Таблица 9 − Классификация подземных вод по общей жесткости
7.4. Химическая классификация подземных вод
Разнообразие химического состава природных вод определяет необходимость их систематизации. Существует довольно много классификаций учитывающих химические свойства, соотношение групп анионов и катионов, генетические особенности вод.
Широко применяется классификация О.А. Алекина (рисунок 10), сочетающая принцип деления по преобладающим ионам и соотношениям между ними. Преобладающим является тот ион (отдельно рассматриваются анионы и катионы) , содержание которого больше каждого из двух других не менее чем на 10 %-экв/л. Если разница меньше, то вода будет смешанного состава, при этом уступающий в пределах 10 %-эквивалентов ион будет читаться сокращенным прилагательным, а преобладающий – полным.
По преобладающим анионам выделяется три класса вод: гидрокарбонатные (C ), сульфатные (S ) и хлоридные (С l ). В каждом классе по преобладающим катионам выделяют группы кальциевых, магниевых, натриевых вод.

Рисунок 10 - Схема классификации природных вод по химическому
Класс гидрокарбонатных вод объединяет маломинерализованные воды рек, пресных озер и значительное количество подземных вод.
К хлоридным относятся минерализованные воды рек, озер, морей, лиманов, подземные воды солончаковых районов, пустынь.
Сульфатные воды занимают промежуточное место между гидрокарбонатными и хлоридными.
По соотношению ионов выделяют четыре типа вод:
I тип . Это пресные, мягкие воды рек, поверхностных водоемов.
II тип . Воды малой и средней минерализации озер, рек, подземные вода, залегающие в осадочных породах.
III тип . К этому типу относятся сильноминерализованные вода глубоких горизонтов, океанов, морей, лиманов.
IV тип. Воды этого типа кислые, сильноминерализованные, очень жесткие.
Состав воды в соответствии с классификацией О.А. Алекина записывают в виде символа, к которому прибавляется и величина минерализации в г/л.
Например : вода гидрокарбонатная кальциевая второго типа с минерализацией 0,88 г/л будет записана символом - C II Ca 0,88
Определив класс, группу и тип вод по классификации О.А. Алекина, записывают их в графу 18 таблицы 6 при помощи символов.